Você pesquisou por:"Paolo Pelosi"
Encontramos (3) resultados para a sua busca.Resumo
Rev Bras Ter Intensiva. 2016;28(2):104-106
DOI 10.5935/0103-507X.20160023
Resumo
Rev Bras Ter Intensiva. 2008;20(2):178-183
DOI 10.1590/S0103-507X2008000200011
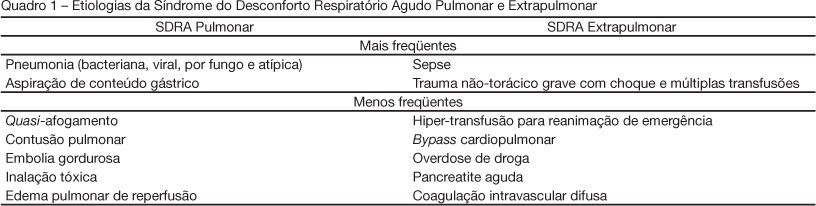
JUSTIFICATIVA E OBJETIVOS: A patogênese da síndrome do desconforto respiratório agudo (SDRA) tem sido explicada pela presença de uma agressão direta (SDRA pulmonar) e/ou indireta (SDRA extrapulmonar) ao parênquima pulmonar. Evidências indicam que a fisiopatologia da doença pode diferir com o tipo de lesão. O objetivo deste estudo foi apresentar breve revisão das diferenças entre a SDRA pulmonar e a SDRA extrapulmonar e discutir as interações entre os aspectos morfofuncionais e a resposta aos diferentes tratamentos. CONTEÚDO: Esta revisão bibliográfica baseou-se em uma pesquisa sistemática de artigos experimentais e clínicos sobre SDRA incluídos nas bases de dados MedLine e SciElo nos últimos 20 anos. Muitos pesquisadores concordam, com base em estudos experimentais, que a SDRA pulmonar e a SDRA extrapulmonar não são idênticas no que diz respeito aos aspectos morfofuncionais, a resposta à pressão positiva ao final da expiração (PEEP), manobra de recrutamento alveolar, posição prona e outras terapias farmacológicas. Entretanto, os estudos clínicos têm descrito resultados contraditórios, os quais podem ser atribuídos à dificuldade de se classificar a SDRA em uma ou outra etiologia, e de se precisar o início, a fase e a gravidade da SDRA nos pacientes. CONCLUSÕES: Pacientes com SDRA de etiologias distintas perduram sendo considerados como pertencendo a uma mesma síndrome e, assim, são tratados da mesma forma. Logo, é fundamental entender as diferenças fisiopatológicas entre a SDRA pulmonar e extrapulmonar para que a terapia seja mais bem direcionada.
Resumo
Rev Bras Ter Intensiva. 2017;29(1):55-62
DOI 10.5935/0103-507X.20170009
Avaliar a atividade antibacteriana contra Staphylococcus aureus e Pseudomonas aeruginosa de dois revestimentos endotraqueais com nanopartículas e fotocatálise sob luz visível.
Testaram-se dois tipos de nanopartículas de titânio: anatase padrão (TiO2) e TiO2 nano-dopada (N-TiO2). As nanopartículas foram colocadas em superfície interna de segmentos de tubos endotraqueais comerciais, aplicadas sobre um filtro de acetato de celulose; os tubos endotraqueais controle foram deixados sem revestimento de nanopartículas. Em cada tubo endotraqueal foi inoculado um total de 150 unidades formadoras de colônia e, a seguir, estes foram expostos a uma fonte de luz fluorescente (3700 lux, comprimento de onda de 300 - 700nm) por 5, 10, 20, 40, 60 e 80 minutos. Contaram-se as Unidades Formadoras de Colônia após 24 horas de incubação a 37ºC. A inativação bacteriana foi calculada como a redução porcentual do crescimento bacteriano em comparação a tubos não expostos à luz.
Na ausência de luz, não se observou qualquer atividade antibacteriana relevante contra qualquer das cepas estudadas. Para P. aeruginosa, ambos os revestimentos tiveram inativação bacteriana mais elevada do que o controle em qualquer dos momentos de avaliação (p < 0,001), sendo que não se observaram diferenças entre o revestimento padrão e nano-dopado. Para S. aureus, a inativação foi maior que os controles, começando a partir de 5 minutos para nano-dopado (p = 0,018) e 10 minutos para o revestimento padrão (p = 0,014); a inativação com a forma nano-dopada foi maior do que com a forma padrão aos 20 minutos (p < 0,001), 40 minutos (p < 0,001) e 60 minutos (p < 0,001).
O revestimento com nanopartículas de titânio comercial padrão e nano-dopado inibiu o crescimento bacteriano sob a luz fluorescente visível. o revestimento nano-dopado teve maior atividade antibacteriana contra S. aureus em comparação à atividade observada com o revestimento com anatase padrão.
